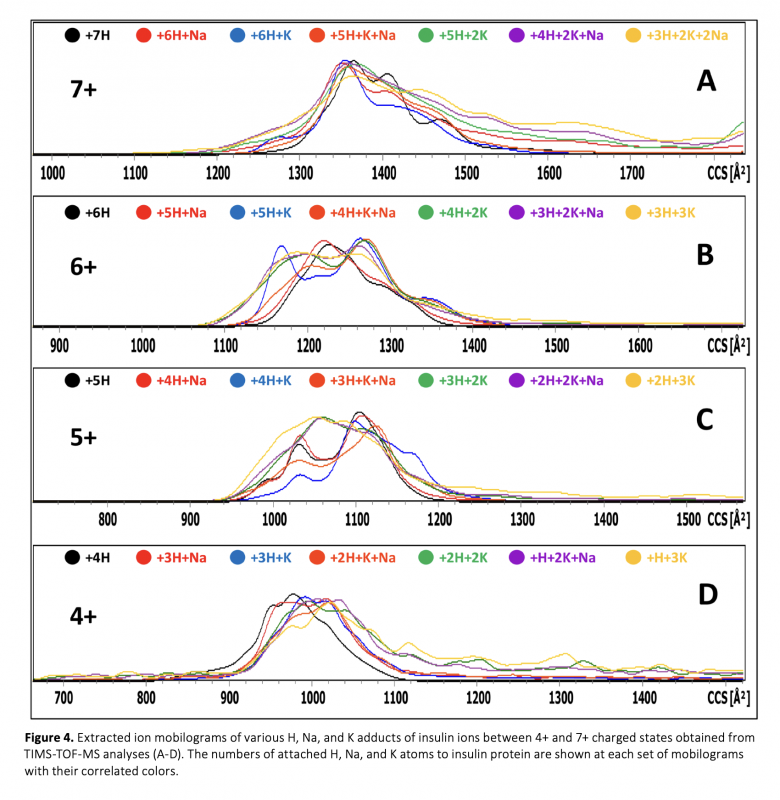
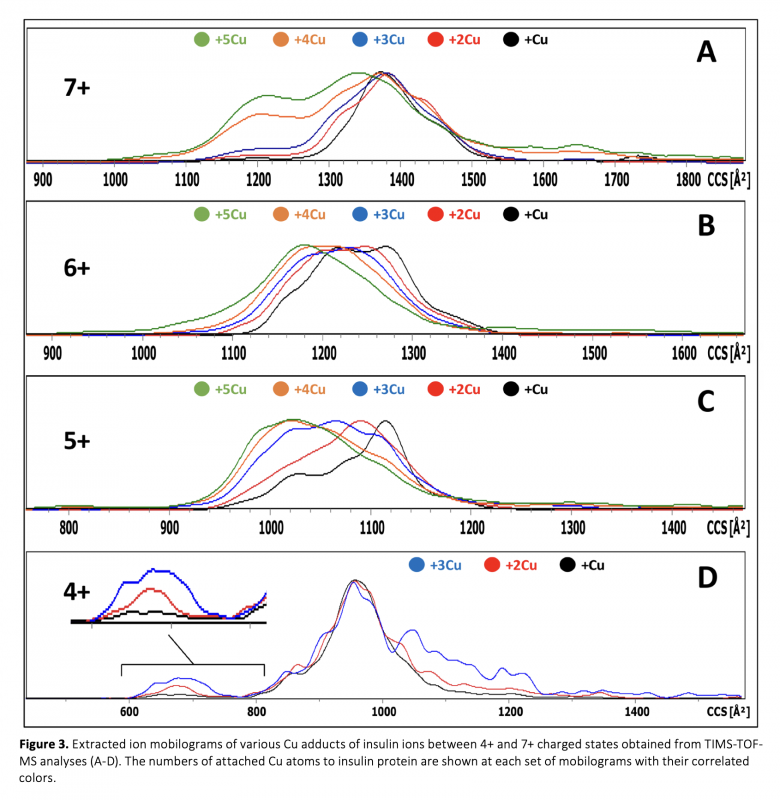
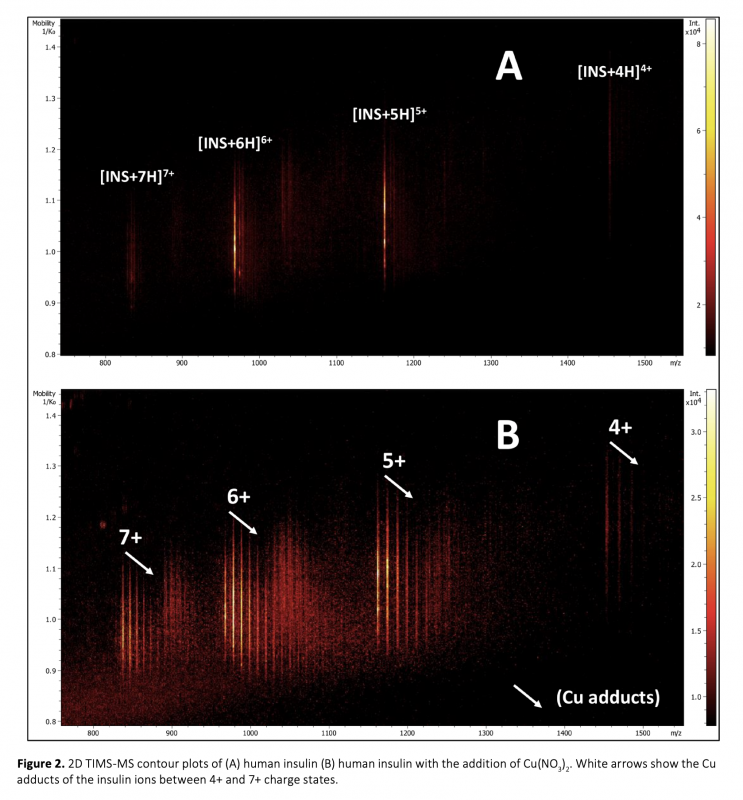
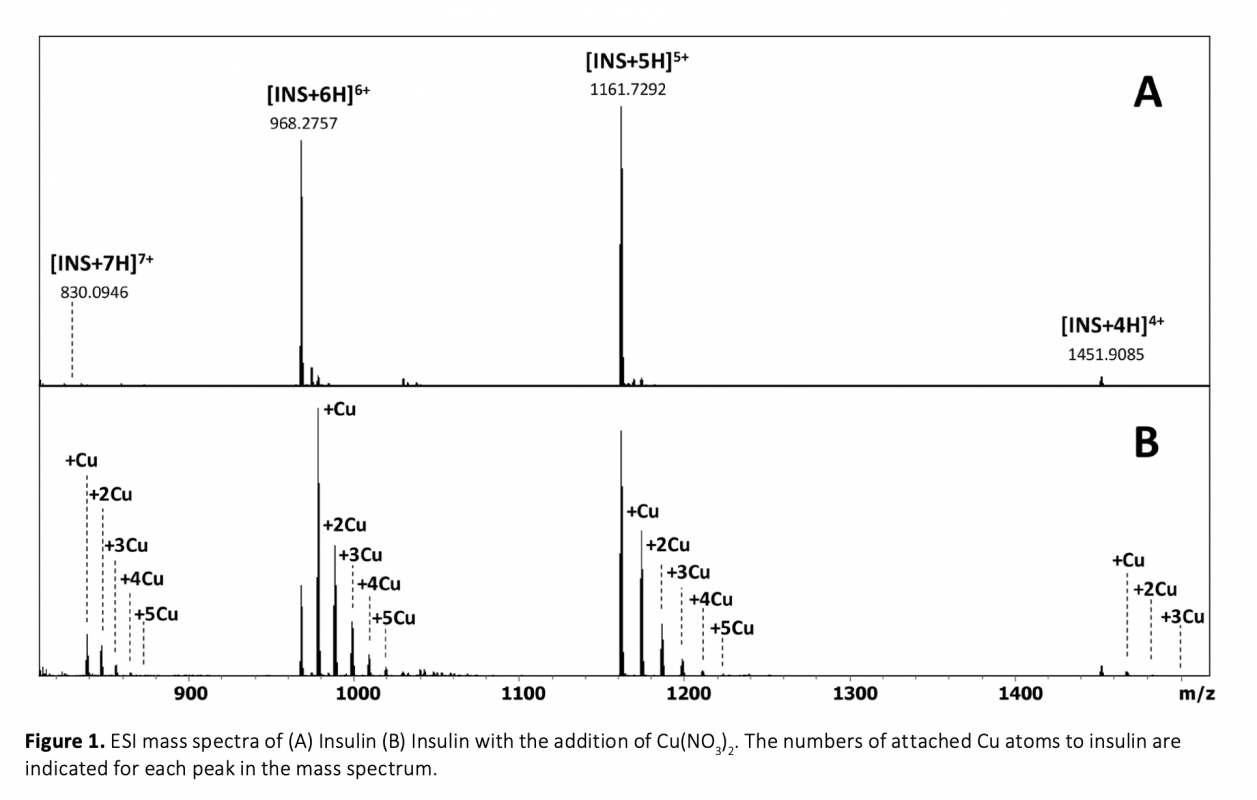
Molecular recognition, protein folding, and formation of supramolecular structures that occur at the molecular level of biological processes are based on noncovalent interactions. Interactions between metal atoms and proteins are also based on noncovalent interactions that underlie the mechanisms involved in many cellular processes. The activities of enzymes are highly dependent on the interactions of such protein groups with cofactors, substrates, metal ions, and other proteins. The compositions and binding stoichiometry of protein-metal complexes can be determined with high accuracy performing mass spectrometry (MS) analysis. The conformational features of protein-metal complexes can be studied additionally using a mass spectrometer with ion mobility spectrometry (IMS) capability. This study focuses the monitoring the differences in the conformational changes of insulin protein during the formation of its complex with copper and alkali metals using trapped ion mobility spectrometry – time-of-flight (TIMS–TOF) mass spectrometer instrument. The compaction of the insulin structure by the formation of the insulin-copper complexes in the gas phase was determined with TIMS-TOF-MS analyses. However, no change was observed in the insulin structure with the addition of H, Na, and K atoms as adducts at the same analysis conditions.
Moleküler tanıma, protein katlanması ve supramoleküler yapıların oluşumu gibi moleküler düzeyde meydana gelen biyolojik süreçler kovalent olmayan etkileşimlere dayanır. Metal atomları ve proteinler arasındaki etkileşimler de birçok hücresel süreçte yer alan mekanizmaların temelini oluşturan kovalent olmayan etkileşimlere dayanmaktadır. Enzimlerin aktiviteleri, bu tür protein gruplarının kofaktörler, substratlar, metal iyonları ve diğer proteinlerle olan etkileşimlerine büyük ölçüde bağlıdır. Protein-metal komplekslerinin bileşimleri ve bağlanma stokiyometrileri, yüksek doğrulukta kütle spektrometrik (MS) analiz ile belirlenebilir. Protein-metal komplekslerinin konformasyonel özellikleri ise iyon hareketliliği spektrometrisi (IMS) özelliğine sahip bir kütle spektrometresi kullanılarak ek olarak incelenebilmektedir. Bu çalışmada tuzaklamalı iyon hareketliliği spektrometrisi - uçuş zamanlı (TIMS-TOF) kütle spektrometresi kullanılarak bakır ve alkali metallerle komplekslerinin oluşumu sırasında insülin proteininin konformasyonel değişimlerindeki farklılıkların izlenmesine odaklanılmaktadır. İnsülin-bakır komplekslerinin oluşmasıyla insülin yapısının gaz fazında daha kompakt hale geldiği TIMS-TOF-MS analizleri ile belirlenmiştir. Ancak aynı analiz koşullarında H, Na ve K atomlarının eklenmesiyle insülin yapısında herhangi bir değişiklik gözlenmemiştir.
Download Article in PDF (3.2 MB)